Neurale Stammzellen und gliale Progenitoren
Biologie neuraler Stammzellen unnd glialer Progenitoren:
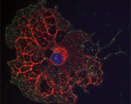
Neurale Stamm/Progenitorzellen, gliale Progenitoren und ihre Nischen entstehen aus einer Schicht von Neuroepithel, die sich durch symmetrische Teilung vermehrt. Mit wachsender Dicke der Wände des Neuralrohrs entwickelt sich das Neuroepithel zur radialen Glia (RG) weiter. Diese proliferiert und erneuert sich durch symmetrische Teilung. Andererseits bildet die RG mit fortschreitender Zeit Neurone, die durch asymmetrische Teilung generiert werden. Hierdurch produziert die RG Neurone in vivo und fungiert als neurale Stamm/Progenitorzelle (NSPC).
Nach der Neurogenese werden Oligodendrozyten Vorläufer (OPC) gebildet, die in ihre Zielregionen wandern, um dort die axonalen Verbindungen zu myelinisieren. Schließlich verwandelt sich die radiale Glia in Astrozyten, mit zwei wohlbekannten Ausnahmen, der Bergmann Glia des Kleinhirns und der Müller Glia der Retina. Im adulten ZNS ist die Neurogenese auf zwei kanonische Regionen beschränkt, die subventrikuläre Zone (SVZ) des lateralen Ventrikels und die Subgranularzone (SGZ) des Hippokampus. Man nimmt an, dass in diesen Regionen die RG in Gestalt radialer Astrozyten weiterbesteht und die Neurogenese des adulten ZNS ermöglicht.
Es wird weiterhin angenommen, dass die neurogenen Regionen aus als Nischen bestehen, die an dem Erhalt der NSPCs beteiligt sind. Diese besitzen eine integrative Funktion für eine große Zahl physiologischer Stimuli. Der LS untersucht die Implikationen dieses Konzepts und fokussiert sich hierbei auf die EZM Bestandteile der Stammzellnische. Besondere Beachtung wird hierbei dem Glykoprotein Tenascin C und den Chondroitinsulfat Proteoglykanen der Nische gewidmet. Die Bedeutung dieser Komponenten für die Differenzierung glialer Vorläuferzellen, vor allem der Astrozyten und der Oligodendrozyten Vorläuferzellen und ihre Bedeutung für die Myelinisierung während der Entwicklung, nach Läsionen und im Rahmen von Krankheitsprozessen stellen Themen der Arbeitsgruppe dar. Ein anderer Aspekt der Arbeit betrifft die Expression dieser EZM-Moleküle in glialen Tumoren und ihre potenziellen Effekte auf Tumorstammzellen des Nervensystems. Schließlich beschäftigt sich die Arbeitsgruppe auch mit der Antwort der Stammzellnische auf Schäden und den potentiellen Nutzen der Stammzellen für die Regeneration und Reparatur des Zentralnervensystems.
Ein weiteres Interessensgebiet stellt die Interaktion der Zelle mit extrazellulären Molekülen dar. Ein wichtiges Beispiel dafür ist ein Transmembranrezeptor, der die Differenzierung von Gliazellen beeinflusst: LRP1 (low-density lipoprotein receptor-related protein 1). Dabei handelt es sich um einen ubiquitär exprimierten Rezeptor mit über 40 potentiellen Liganden, wie Integrinen, Matrixmolekülen und verschiedenen Wachstumsfaktoren. Am Lehrstuhl wird die Funktion dieses Rezeptors in der Entwicklung des zentralen Nervensystems vor allem im Hinblick auf Gliazellen thematisiert, wobei radiale Glia, Astrozyten und Oligodendrozyten im Fokus stehen.
Aktuelle und frühere Förderungen:
DFG (Fa 159/16-1 / vHo 2476/1-3), BMBF, Mercatorstiftung und Land NRW.
Mitglieder