Teilprojekt C: Prof. Dr. M. Havenith-Newen
Ruhr-Universität Bochum
Hochauflösende IR-Spektroskopie von ultrakalten molekularen Aggregaten
Ziel der Arbeiten ist es, mithilfe der hochauflösenden IR-Spektroskopie in supra-flüssigen Heliumnanotröpfchen die Struktur von molekularen Aggregaten zu bestimmen. Die nun in Bochum einzigartig zur Verfügung stehenden Möglichkeiten: Hohe Nachweisempfindlichkeit verbunden mit massenselektiver IR-Depletion-spektroskopie bei hoher spektraler Auflösung (0.001 cm-1) soll in diesem Antrag systematisch weiter ausgebaut werden und konsequent für die Themenstellung der Forschergruppe genutzt werden. Dabei werden die inzwischen etablierten guten Kooperationen innerhalb der Forschergruppe als wesentlich für einen Erfolg angesehen.
Insbesondere sollen die beiden folgenden Teilaspekte ausführlicher behandelt werden:
1. Einfluss der Deuterierung und der Fluorierung auf die Aggregation von Pyridenkomplexen. Da sich bei Kristallstrukturuntersuchungen von Boese et al. (Teilprojekt A) interessante Änderungen des Packungsverhaltens bei lokaler H/D Substitution zeigte, möchten wir systematisch den Einfluss der Isotopensubstitution auf die Struktur der Dimere untersuchen. Wie sich bei vorhergehenden MW-Studien zeigte, wird durch partielle F-Substitution an den unterschiedlichen Stellen im Ring gezielt der Pyridinring in seiner Geometrie beeinflusst.[14] Gleichzeitig wird die Ladungsverteilung im Ring selektiv geändert. Bei H/D Substitution ändert sich die Energie der Nullpunktschwingung. Der Einfluss von beiden Effekten auf die Aggregation der Komplexe soll Gegenstand der hier vorgeschlagenen Untersuchungen sein. Dazu soll Pyridin und Pyridendimer im Bereich der asymmetrischen C-H Schwingung bei 3200 cm-1 untersucht werden. Analog zu den Arbeiten im letzten Antragszeitraum möchten wir hierbei massenselektive, hochauflösende IR-Spektren aufnehmen. Diese Arbeiten werden in enger Anlehnung an die Teilprojekte A und G erfolgen. Für die Untersuchung der partiell substituierten D/F Pyridinderivate können wir direkt auf die Expertise von Herrn Dr. Merz zurückgreifen, der uns die für die Spektroskopie erforderlichen Substanzmengen innerhalb der Forschergruppe zur Verfügung stellen wird.
Ziel ist es, die IR-Spektren einzelner Aggregate zu beobachten. Wir möchten dabei folgende Fragen beantworten: a) Welche Konformere (und wie viele) können beobachtet werden? b) Welche Banden können wir dem Dimer zuordnen, wieweit sind diese gegenüber der Monomerbande rot- bzw. blauverschoben? c) Ist es möglich bei einzelnen IR-Banden die Rotationsstruktur aufzulösen, bzw. können daraus Rückschlüsse auf die Rotationskonstanten der Dimere gezogen werden? d) Wie vergleichen sich die erhaltenen Dimerstrukturen mit den theoretischen Vorhersagen und den in der Matrix bzw. im Kristall beobachteten Strukturmotiven? e) Welche Schlussfolgerungen können wir daraus bezüglich des Einflusses von Isotopensubstitution und der Änderung der Ladungsverteilung auf die Aggregat-bildung ziehen?
2. Mikrosolvation von Säuren Wir möchten die in der ersten Periode begonnene Untersuchung der aggregations-induzierten Autodissoziation von HCl in kleinen Wasseraggregaten HCl-(H2O)n zunächst zu Ende führen. Dazu sollen die erhaltenen Spektren weiter ausgewertet werden und mit den Modellierungen verglichen werden. Wir möchten anhand von weiteren Banden klären, welche Struktur für HCl-(H2O)4 vorliegt und möchten zusätzlich noch Vibrationsübergänge im Bereich der HCl und H3O+ Bande für Cluster mit n=2,3 oder >4 im Spektrum suchen.
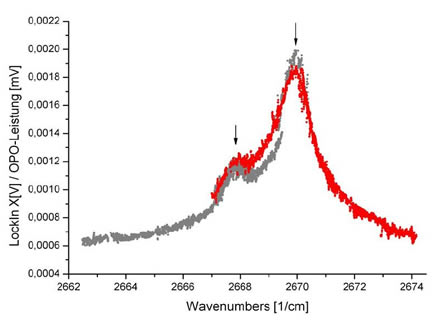
Spektrum von (HCl)n-(H2O)m-Clustern bei niedrigem HCl-Druck und mittlerem Wasserdruck. Es sind zwei Linien bei ca. 2270 und bei 2668 cm-1 zu erkennen. An den durch Pfeile gekennzeichneten Positionen wurden optisch selektive Massenspektren aufgenommen.
Weiterhin soll in Zusammenarbeit mit der Gruppe Marx der Effekt der Isotopensubstitution untersucht werden, um zu klären, ob die Deuterierung Einfluss auf den Dissoziationsmechanismus hat. Wir möchten dann nachfolgend diese Untersuchungen zur Mikrosolvatation auf Aminosäuren am Beispiel von Arginin und Phenylalanin ausdehnen. Dabei möchten wir insbesondere der Frage nachgehen, wann diese als neutrale, kanonische Form und wann als Zwitterion vorliegen. Insbesondere soll dabei wieder die Anzahl der Wassermoleküle beim Aggregat systematisch erhöht werden, um zu klären, wie viele Wassermoleküle für den Übergang erforderlich sind, wobei die beim Arginin bereits für das Monomer Gegenstand von Diskussionen ist.
Im Heliumnanotröpfchen kommt es zu einer Aggregation von ultrakalten Monomeren. Dadurch ist es möglich, neben einer infrarotspektroskopischen Charakterisierung der Struktur im globalen Minimum der Potentialfläche, wie sie immer bei Aggregation im Molekularstrahl (Gasphase) erhalten wird, auch andere zusätzliche Strukturen zu beobachten. Im Heliumnanotröpfchen werden beim sukzessiven Einfang von zwei Monomeren diese zunächst im suprafluiden Helium auf 0.37 K abgekühlt bevor es zur Aggregation kommt. Bei der Annäherung überwiegt bei größeren Abständen die Dipol-Dipolwechselwirkung, da diese von den intermolekularen Wechselwirkungen die langreichweitigste ist. Es kommt daher zunächst bevorzugt zu einer linearen Ausrichtung der beiden beteiligten Dipole (head-tail configuration). Falls diese Struktur einem lokalen Minimum auf der Potentialfläche entspricht, müsste bei weiterer Annäherung eine Potentialbarriere überwunden werden, um zum globalen Minimum zu gelangen. Dies ist aber in vielen Fällen nicht möglich, da bei 0.37 K nicht genügend thermische Aktivierungsenergie zur Verfügung steht. Ähnliche Effekte können daher auch in der Matrixspektroskopie (Teilprojekt G, Sander) beobachtet werden, wobei dabei aber wieder zusätzliche Energie beim Tempern der Matrix zugefügt werden kann, und die Umgebungs-temperatur mit 8-10 K bzw. 25-30 K höher ist als im ultrakalten Heliumnanotröpfchen. Wir möchten daher für die geplanten Projekte auch der Frage nachgehen, wodurch die Aggregatbildung bei ultrakalten Temperaturen gesteuert wird.